接觸氧化除鐵規律的研究
| 論文類型 | 技術與工程 | 發表日期 | 2001-07-01 |
| 來源 | 賀李圭白院士七十壽辰學術論文集 | ||
| 作者 | 李繼震 | ||
| 關鍵詞 | 氧化除鐵 | ||
| 摘要 | 在試驗和生產的基礎上,對現在普遍采用的接觸氧化除鐵基本方程式進行修正和補充,提出新的基本方程式,建立了除鐵水含鐵量與濾池工作時間的函數關系,并指出系數n的影響因素。此外,還對濾潛水鐵質的形態對除鐵效果的影響、pH值的變化和濾料總表面積與除鐵水水質的關系等規律作了探討。 大多數地下水除鐵水廠都采用接觸氧化除鐵方法。新濾料投產后有一段成熟期,成熟后的濾料依靠活性濾膜除鐵,而濾料本體僅在成熟期中有一定的化學和物理作用,在正常生產中僅為活性濾膜的載體使用。活性濾膜具有強烈且穩定的接觸氧化除鐵作用,因而具有接 | ||
李繼震
摘 要:在試驗和生產的基礎上,對現在普遍采用的接觸氧化除鐵基本方程式進行修正和補充,提出新的基本方程式,建立了除鐵水含鐵量與濾池工作時間的函數關系,并指出系數n的影響因素。此外,還對濾潛水鐵質的形態對除鐵效果的影響、pH值的變化和濾料總表面積與除鐵水水質的關系等規律作了探討。
大多數地下水除鐵水廠都采用接觸氧化除鐵方法。新濾料投產后有一段成熟期,成熟后的濾料依靠活性濾膜除鐵,而濾料本體僅在成熟期中有一定的化學和物理作用,在正常生產中僅為活性濾膜的載體使用。活性濾膜具有強烈且穩定的接觸氧化除鐵作用,因而具有接觸氧化除鐵的獨特規律。根據試驗研究的結果和對生產現象長期的觀察,本文就接觸氧化除鐵的一些規律,作以論述。
1.1 現行接觸氧化除鐵基本方程式
現在被人們普遍采用的接觸氧化除鐵基本方程式為
![]() (2)
(2)
![]() ; (3)
; (3)
式中 β —接觸氧化除鐵活性系數
β′—除溶解氧、濾速、粒徑之外,其他因素影響的除鐵活性系數
р—指數,取決于水的運動狀態,其值在0~1范圍內,可由試驗確定
式中反映出鐵水含鐵量[Fe2+]與原水中含鐵量[Fe2+]0、濾層深度x、當量粒徑d、原水溶解氧濃度[O2]、濾速v之間的函數關系,能夠深刻反映出某一時刻除鐵的規律,但是,實際上在不同時刻除鐵水的含鐵量是不同的,隨著濾池工作時間而有規律的變化(見圖1),這些變化在公式中沒有體現出來。
1.2 [Fe2+]隨時間T變化的原因及規律
接觸氧化除鐵的水化學反應過程是Fe(OH)3•2H2O作為催化劑的表面自動接觸催化過程,所以催化能力的大小與附著在濾料表面(與水接觸部分)Fe(OH)3•2H2O的數量成正比,反沖洗后剛投入運行濾池的濾料表面,只保留少部分必要的具有催化活性的Fe(OH)3•2H2O濾膜,而大部分濾膜在反沖洗中被沖掉了,由于數量有限,所以除鐵效果較差。又因為除鐵過程式自動接觸催化反應,所以隨著工作時間T的增長,濾料表面上生成并積累的Fe(OH)3•2H2O的數量不斷增多,催化能力不斷增大,除鐵效果也越來越大。
通過幾個月的濾管試驗,得出了出水含鐵量與過濾時間的關系,以其中一組為例進行探討。d=1.585mm、K<1.3、H=0.83m、[Fe2+]=10mg/L、v=7.3m/h、pH=6.2、水溫6℃、[O2]=8mg/L,除鐵水含鐵量與時間的關系見圖1。
從圖中可以看出,除鐵水含鐵量隨著反沖洗后濾池的工作時間而有規律的變化著。
1.3 基本方程式的建立
由式(3)得
![]()
![]() (4)
(4)
根據試驗得到的數據,利用式(4)進行計算,得出試驗中各不同時刻濾料的除鐵活性系數 β ,繪出 β 與T的關系曲線,見圖2。
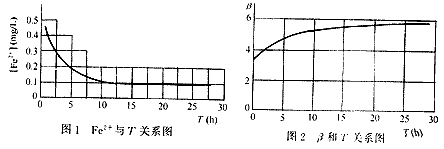
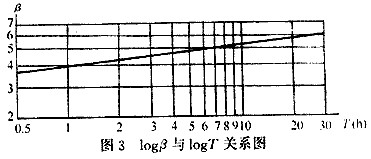
圖2中,β為時間T的函數,進一步建立logβ與kogT 的關系圖像,見圖3。
圖3的圖像為一條直線,建立該直線的方程式
log β-log β1=n(logT-log1)
式中 n——直線的斜率,本組實驗n=0.123
β1——反沖洗后濾池工作1h(即T=1),濾池的除鐵活性系數
β——反沖洗后濾池工作T小時,濾池的除鐵活性系數
整理上式
log β=log β1+nlogT
log β=lpg β1Tn
β= β1Tn
將式(5)分別代入式(3)、(2)、(1)得
![]()
![]()
![]()
式中β′—反沖洗后濾池工作時間1h,除溶解氧、濾速、粒徑之外,其他因素影響的除鐵活性系數。
該方程式反映了出鐵水含鐵量與包括濾池工作時間在內的多元函數關系,即可用來深入理解除鐵的規律,又可以用來做具體計算。
1.4 對n值的探討
對于既定的濾床、原水水質和濾速,n值為常數。對于不同的濾床、原水水質和濾速,n值均有所差異。從50余組試驗中,將具有典型意義的5組試驗得出的n值,列于表1。
表 1 n值統計表
序號
當量粒徑mm
原水含鐵量mg/L
濾速m/L
n
1
1.256
14.2
15
0.116
2
1.585
14.2
15
0.110
3
1.585
10
7.3
0.123
4
1.585
10
12.8
0.118
5
1.256
10
12
0.129
分析水中數據,可得出如下結論:
1)原水含鐵量相同、濾速相同,粒徑越大、n值越小,如1組與2組、4組與5組。
2)原水含鐵量相同、粒徑相同, n值越小,如3組與4組。
3)粒徑相同、濾速相同,原水含鐵量越大、 n值越小,如2組與4組。
總之,粒徑越大、濾速加大、原水含鐵量加大時,n值減小。
2.1 原水中三價鐵對處理效果的影響
與自然氧化法相反,接觸氧化除鐵法希望曝氣后地下水中二價鐵在位敬仰花錢直接進入濾層。假如濾前水中三價鐵所占比例過大,能嚴重影響除鐵效果。在同一濾床中作了對比試驗,見表2。
表2 三價鐵對接觸氧化除鐵效果影響對比表
序號
濾層當量粒徑cm
原水含鐵量mg/L
濾速
m/h
出水平均含鐵量mg/L
除鐵百分比%
總鐵
三價鐵
二價鐵
三價鐵占總鐵
總鐵
三價鐵占總鐵
二價鐵
三價鐵
總鐵
1
1.256
10
0.9
9.3
9
14
0.143
70
99.53
89
98.57
2
1.256
6
2.0~2.8
2.2~4
33~47
10
0.3
65~70
96~97.4
90~92.5
95
從表中可以看出,第二組試驗與第1組試驗相比,盡管原水總含鐵糧由10mg/L降到6mg/L,濾速由14m/h降到10m/h,但是出水含鐵量反而增加了一倍多,由0.143mg/L增高到0.3mg/L,其原因是原水中三價鐵的存在的比例過大造成的影響。從而說明了,三價鐵對接觸氧化除鐵不但沒有益處反而還有害處。
2.2 討論
上述特征的存在,是由于接觸氧化除鐵原理所決定的。濾料表面的活性濾膜的主要成分是對水中Fe2+的氧化起接觸作用的Fe(OH)3•2H2O,該化合物能與水中Fe2+進行離子交換吸附,其反應為:
Fe(OH)3.2H2O+Fe2+→Fe(OH)2.O.Fe2+.2H2O+H+
生成Fe2+與Fe2+的黑色復合物,在水中含有溶解氧時能迅速的進行水解和氧化反應,其反應為
Fe(OH)2.O.Fe+.2H2O+1/4O2+9/2H2O→2[Fe(OH)3.2H2O]+H+
又生成了新的Fe(OH)3•2H2O,所以其接觸氧化除鐵過程是一個自動催化反應過程,因而除鐵效率非常高。水中三價鐵在中性條件下是以氫氧化物沉淀形式存在的,而Fe(OH)3•2H2O不能與水中三價鐵進行離子交換吸附,濾料對水中三價鐵沉淀物的去除只能起到機械過濾作用,而且三價鐵沉淀物沒有很好的絮凝,因而去除效率低。從表2看出,原水中三價鐵含量占總鐵含量由9%增加到33~47%時,除鐵效率由99.57%降為95%,同時對其中三價鐵的去除率僅為90%左右。
此外,自然氧化生成的三價鐵沉淀物,沒有嚴密的化學結構,其分子式可用Fe(OH)3•nH2O表示,一般不具有接觸氧化活性,所以與具有特殊結構的活性濾膜物質是不同的。從外觀上,自然氧化生成的三價鐵氫氧化物沉淀為土黃色,而在活性濾膜上生成的三價鐵化合物為棕褐色,有明顯不同。在過濾前的水中自然氧化生成的三價鐵沉淀物進入濾池后,會附著在濾料表面積上,減少了具有強烈活性濾膜的表面積,影響了其對地下水中二價鐵的去除能力。從表2中可以看出,原水三價鐵含量由9%增加到33~47%時,使其中二價鐵的去除率由99.53%降到96~97.4%。總之,濾前水中三價鐵含量過大,對接觸氧化除鐵的效率影響很大。在這種濾前條件下,為了得到合格得出鐵水,就必須大幅度降低濾速。
3.PH值的變化
自然氧化法除鐵,水在曝氣過程中pH值有所上升,在濾床中滲透時pH值不變。而接觸氧化法除鐵則情況有所不同,水在曝氣時pH值有所提高,在濾床中滲濾pH值則有所下降。
由前述的接觸氧化除鐵反應方程式中可以看出,每個Fe2+離子可以置換出兩個H+離子。假如原水含鐵量為14mg/L,可置換出的氫離子濃度為0.5mgq/L,其數量相當可觀。地下水是一種比較復雜的緩沖溶液,主要是碳酸鹽和酸式碳酸鹽構成的緩沖溶液,因而被置換出來的氫離子只能使在一定程度上使H+濃度增加、pH值降低,pH值下降的幅度一般可達0.2~0.4,這是不可忽視的變化。
依據濾前水的水質,可求出濾過水pH值,其計算式為
pH=pKa+log[HCO3-]-2[Fe2+]M)-log([H2CO3]+2[Fe2+]M (9)
式中 Ka——級碳酸電離平衡常數
[Fe2+]M —原水中二價鐵的摩爾濃度
[HCO3-]、[H2CO3] —過濾前水中的[HCO3-]、[H2CO3]摩爾濃度
但是,實際上碳酸有可能被活性濾膜吸附,結果使計算得到的pH值產生誤差,被吸附的二氧化碳數量難以確定,卻引起的計算偏差也難以求得。實際上,計算出的pH值總是比實際值略低。
4. 濾料的總表面積與降鐵水質的關系
每m2濾池面積里,濾料的總表面積為
[6(1-m)/φ].(x/d)
濾料選定后,其孔隙率m、球形度Φ為定值,則總表面積s是濾層深度x與當量粒徑d的比值x/d的函數。
基本方程式(8)中,指數中的x/d即體現濾層的總表面積,而常數6(1-m)/Φ可以看作包含在系數β中,則濾料總表面積是決定接觸氧化除鐵效果的重要因素。式(8)反映出濾過水含鐵量與x/d的函數關系,可為設計和生產提供較準確的數據。實驗資料表明,同一水質,不論是一般濾床、反粒度濾床或者是均勻粒徑濾床,只要s相同,即x/d相同,則除鐵效果基本相同。但是,應指出,盡管它們的出鐵效果一樣,但是水力條件則各不相同,體現在水力損失及其增長的規律、含污能力、可選用的濾速及相應的工作周期等都各有不同。生產中,筆者曾選用大粒徑均勻濾料,佳木斯自來水公司曾選用反粒度濾料,都是在s基本一樣,除鐵效果基本不變的前提下,取得了改善濾床的水力條件,增加濾池的含污能力,提高濾速,從而達到了提高處理水量的目的。
參 考 文 獻
[1] 李圭白、劉超,“地下水除鐵除錳”,中國建筑工業出版社,1989年
相關推薦
論文搜索
月熱點論文
論文投稿
很多時候您的文章總是無緣變成鉛字。研究做到關鍵時,試驗有了起色時,是不是想和同行探討一下,工作中有了心得,您是不是很想與人分享,那么不要只是默默工作了,寫下來吧!投稿時,請以附件形式發至 paper@h2o-china.com ,請注明論文投稿。一旦采用,我們會為您增加100枚金幣。








