電化學法測定生物活性
| 論文類型 | 技術與工程 | 發表日期 | 2006-12-01 |
| 來源 | 中國水網 | ||
| 作者 | 宋亞文,季民,伍洋,呂鳴祥 | ||
| 關鍵詞 | 電化學法 微生物電極 生物活性 | ||
| 摘要 | 探討了應用生物傳感電極法測定微生物優勢酶活性的可行性。以三乙醚三甘油酯及豆油乳液作為底物,通過測定微生物電極對底物的響應電流來測定微生物體內酯酶及脂肪酶(系)的活性。應用該方法測定厭氧和好氧反應器內生物膜及懸浮污泥的酶活性時發現,測出的酶活性量大小與單位質量污泥的有機物擊除負荷緊密相關。在UASCB-MBBR串聯系托中.好氧反應器中生物酶活性高于壓氧反應器;在UASCB中,上部厭氧生物膜中酯酶活性高于厭氧污泥,而脂肪酶活性則是底部污坭床的污泥高于上部生物膜;在MBBR中,生物膜的酯酶及脂肪酶活性均高于懸浮 | ||
1 引言
廢水生物降解的實質是,基質通過活性污泥或生物膜中微生物細胞分泌的各種酶系的催化而逐步被氧化分解的過程.其中,催化劑以氧化還原酶系最為主要。因此,根據不同水質條件下微生物所產生的優勢酶特性,可通過測定酶的催化能力大小來衡量微生物的活性。
對于生物活性的測定分析,尚無統一的定量標準。目前提出的一些方法,如ATP法、脫氫酶法等,測定技術都比較復雜,過程也難以控制,不利于實際生產中推廣應用。
利用電化學的方法,運用微生物傳感電極測定活性,目前在國內外文獻中報道較少,本文將對此進行初步的研究和探索。
2 試驗原理
微生物活性是以微生物體內優勢酶系的活性來表征的。由于酶的活性大小可由一定條件下它所催化的某一化學反應的反應速度來表示,所以酶的活性高低(實質上是酶的定量測定)表現在酶促反應的速度,即單位時間內底物或產物濃度的變化。
酶促反應符合米氏公式,則有:

式中:V—— 酶促反應的反應速度;
vm——酶促反應的最大反應速度
Km——米氏常數;
s— — 底物濃度;
i——響應電流,與反應速度相一致。反應速度越快,響應電流越大。
在一定范圍內,1/i∝1/s呈線性關系,這個范圍也稱之為線性范圍。隨著s值的增大,i趨向于一個極限值,即底物濃度無限大時,達到了酶促反應的最大反應速度vm 。
米氏常數K 表征了酶與底物的親和力大小,它是酶自身所決定的,與溫度、pH值、酶自身特性均有關。K 越小,酶與底物的親和力越強。而酶促反應的最大速度vm則反映了酶活性的高低,vm越大,則酶活性越高。因此,微生物電極的活性主要采用酶促反應的最大反應速度vm表征。
3 試驗方法
本試驗以天津某食品公司冰淇淋生產廢水作為原水,生物處理主工藝為升流式厭氧污泥復合床(UASCB)一移動床好氧生物膜反應器(MBBR)。對試驗原水水質的初步分析表明,冰淇淋廢水中富含油脂和脂肪。油脂和脂肪的典型代表物為三乙酸三甘油酯和豆油乳液。試驗中以配制的三乙酸三甘油酯和豆油乳液作為底物來測定微生物體內所含的酯酶和脂肪酶(類),得到了較好的響應曲線。
3.1 電極響應特性的測試
通過測量化學反應體系的電流(密度)、電量、電極電位和電解時間等因素之間的函數關系來研究電極過程時,只需要簡單的儀器設備,便能獲得有關的電極過程動力學的參數。循環伏安法(CV法)是目前研究電極過程常用的方法。
本試驗主要栗用CV法,其電化學測試線路如圖1所示。實驗過程中介體為氧氣時,其電位范圍一般為250±500mV;介體為二甲胺基甲基二茂鐵時,電位范圍為100~400mV;介體為苯醌時,電位范圍為100~400mV;介體為鐵氰酸鉀時,電位范圍為550mV。電極掃描速度為25~100mV/s。實驗中采用電解液為pH=6.0,7.5,8.0的0.2mol/L PBS緩沖溶液和pH=5.0 5.6的0.2rnol/L檸檬酸鹽緩沖溶液。
所有實驗數據均為穩定后所測,

電解池采有三電極體系,研究電極為鉑片,面積為0.2cm ,參比電極為飽和甘汞電極(PTFE),輔助電極為鎳絲,鉑電極結構如圖2所示。文中所有電板電位均指對于飽和甘汞電極(SCE)而言。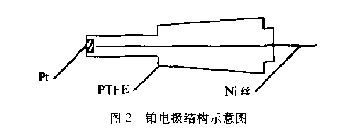
3.2 電極預處理
將燒結好的Pt電極用5#金相砂紙打磨,然后用Al2O3拋光粉拋光至鏡面,在超聲波清洗器中清洗5min后將電極浸泡在lmol/LH2SO4溶液中煮沸5~10min,取出后將電極用二次蒸餾水洗滌,最后在lmol/LH2SO4溶液中以100mV/s速度在一250~250mV范圍內對電極進行線性電位掃描,直至得到通常Pt電極的循環伏安圖,且曲線穩定不再變化為止.取出用二次蒸餾水洗滌、待用。
3.3 微生物電極的制備
3.3.1 醋酸纖維素(CA)基膜的制備
醋酸纖維素是一種羥基聚合物,是沒有強烈氫鍵的無定形鏈狀高分子化合物。它是一種非常優秀的制膜材料,具有很好的成膜和使用性能,這種材料制膜的潛力遠遠高于現在對它的認識。通過對CA作某些化學改性,能制備出新型膜。CA生物活性膜的形成采用了溶出一凝凍法,其和備過程如下:以二氯甲烷為溶劑于30℃ 下攪拌溶解CA,按配方加入無水乙醇、1,6.己二胺、并緩慢滴加50% 戊二醛溶液快速攪拌狀態下反應1.5h。 在一定的溶劑蒸發條件下,將制膜液澆鑄于10cm×10cm帶罩光滑平板玻璃上,均勻展開,流延成膜,靜置24h。待溶劑完全蒸發后,將膜小心的揭下,煮沸5~10min后即可待用。
3.3.2 微生物電極的制備
從填料上刮下附著生長的微生物膜或吸取含活性污泥的懸浮液,取樣的生物量均為5mg左右,滴加于基膜上,真空抽濾5~10min,外面再包覆一層基膜以防測試中微生物流失,用0型圈固定在Pt電極表面,制得微生物電極結構如圖3。

3.4 豆油乳液的配制
稱取2gPVA熱溶于80mL蒸餾水中.定容于100mL。量取13mL豆油與之混合.于恒溫0~5℃冰水浴中超聲波乳化約8h.儲存于冰箱中待用。
4 結果與討論
本試驗所制備的電極中的微生物分剮來自好氧生物膜、好氧懸浮污泥、厭氧生物膜和厭氧生物污泥。當進水容積負荷相同時,分別選取脂肪酶(系)和醇酶作為待測優勢酶表征微生物電極活性,電極性能優劣如附表所示。
從附表可以看出,無論是以三乙酸三甘油酯還是以豆油乳液作為底物,好氧微生物電極的vm值都遠高于厭氧微生物電極。這表明好氧微生物電極的活性遠遠高于厭氧微生物電極活性。對比測試微生物的CODcr去除情況時還發現,進水容積負荷較低時,好氧微生物的活性較低,表明該系統中厭氧處理部分去除了廢水中大部分的CODcr,抑制了好氧微生物活性,使其處于饑餓狀態。這些與測試結果吻合,也就是說,證明了微牛物電極活性與微生物的其他活性參數有著良好的相關性。
附表:電極性能測試結果
待測優勢酶對應底物 三乙酸三甘油酯 豆油乳液 性能參數 vm/μA 線性范圍/mmol km/μA vm/μA 線性范圍/mmol km/μA 厭氧 生物膜 33.6 10 8.3 20.55 0.8 1.73 微生物 生物污泥 11.12 6 2.71 33.79 0.7 9.508 好氧生物膜
75.58 20 22.6 128.5 7 22.62 微生物 懸浮污泥 35.46 25 23.37 86.36 1.8 9.07 此外,試驗中還發現,好氧反應器內生物膜中酯酶和脂肪酶(類)的活性均高于其在懸浮污泥中的活性;厭氧反應器的生物膜中酯酶活性也高于其在厭氧污泥中的活性,而脂肪酶(類)活性卻較厭氧污泥中低。這表明,厭氧處理時.污水中的酯類化合物主要為厭氧反應器上層的生物膜所分解,而脂肪酸則主要被UASCB下部污泥床的厭氧污泥所礦化。好氧處理時,懸浮污泥的密度大干填料,在能夠維持填料轉動的最小氣量下,污泥集中在反應器下部,使得填料與污水的接觸機會大大高于懸浮污泥,因而2種優勢酶(系)在生物膜中的活性都高于懸浮污泥中的活性。

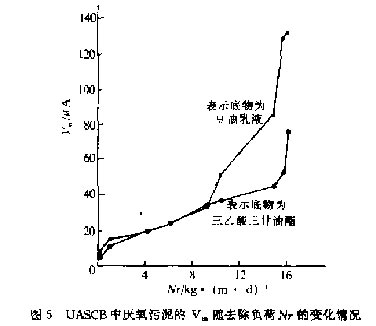
真實廢水中的優勢酶系為脂肪酶(類)和酯酶。由于測定厭氧和好氧微生物電極響應時采用了不同的介體,為了減少由此帶來的誤差,我們將兩部分分開來討論。圖4、圖5所示分別為厭氧和好氧反應器中vm隨去除負荷Nr增大的變化曲線。
從圖中可以看出,微生物優勢酶系的活性與去除負荷具有相同的增減趨勢;對應相同去除負荷的微生物電極.去除率高時,所對應電極的米氏常數Km值較小;厭氧去除負荷在15kg/m d時,無論是醋酶還是脂肪酶.其活性都發生了突變。根據在冰淇淋廢水處理中的試驗結果,厭氧去除負荷在15kg/m3·d時.其容積負荷亦為15kg/m3·d左右.試驗測試表明,在此容積負荷下,CODcr去除率達到最大值,說明酵活性最高時,微生物的新陳代謝達到旺盛的頂點,有機物的去除最快,因而CODcr去除率也達到最大。
因此,以微生物優勢酶系活性作為測定參數的方法將大大簡化生物膜(污泥)括性測定的試驗步驟,對實現污水生物指標實時監測具有重要意義。
第一作者宋亞文.女,1971年出生。畢業于天津大學環境工程專業.工學碩士,工程師.現在北京市市政工程設計研究總皖工作。
論文搜索
發表時間 至
月熱點論文
論文投稿
很多時候您的文章總是無緣變成鉛字。研究做到關鍵時,試驗有了起色時,是不是想和同行探討一下,工作中有了心得,您是不是很想與人分享,那么不要只是默默工作了,寫下來吧!投稿時,請以附件形式發至 paper@h2o-china.com ,請注明論文投稿。一旦采用,我們會為您增加100枚金幣。








