高含量氯化物污水校正系數法測定COD的探討
| 論文類型 | 技術與工程 | 發表日期 | 2002-07-01 |
| 來源 | 土木工程學會水工業分會排水委員會第四屆第一次年會 | ||
| 作者 | 侯雅麗,吳國菊,劉振江,馮大成 | ||
| 摘要 | 侯雅麗 吳國菊 劉振江 馮大成 天津經濟技術開發區污水處理廠 1 前言 天津經濟技術開發區污水處理廠是天津濱海新區第一座污水處理廠。日處理污水十萬噸,全套設備從挪威引進,引進SBR工藝整體技術和關鍵設備。經過幾個月的試運行出水水質達到國家排放標準。該廠的建成對進一步改善投資環境,減輕 ... | ||
侯雅麗 吳國菊 劉振江 馮大成
天津經濟技術開發區污水處理廠
1 前言
天津經濟技術開發區污水處理廠是天津濱海新區第一座污水處理廠。日處理污水十萬噸,全套設備從挪威引進,引進SBR工藝整體技術和關鍵設備。經過幾個月的試運行出水水質達到國家排放標準。該廠的建成對進一步改善投資環境,減輕渤海水域的污染壓力起到積極的作用。而開發區特殊的地理位置(未開發前是一片鹽灘),決定了流進污水廠的污水,其氯化物含量是相當高的。如何消除采用重鉻酸鉀法測定COD時,氯化物對COD值的影響是我們化驗室人員必須面對的課題。
化學需氧量(CODcr)是指在強酸性溶液中,一定量的重鉻酸鉀氧化水樣中的還原物質,所消耗氧化劑的量。它是衡量水體中有機物相對含量的重要指標。對于污水處理廠的效果評價它是一個重要而易得的參數。
采用重鉻酸鉀標準方法測定,消除氯化物的干擾,一般采用添加硫酸汞使之與Cl-反應生成可溶性難離解的氯化汞絡合物的方法。該方法操作簡便,但汞鹽對環境造成二次污染。
我廠生化處理前的水CODcr值在330~410mg/L,Cl-值在1600~2000mg/L。廢水經生化處理后,有機物大部分被分解,出水COD值在90~130mg/L,Cl-值沒有變化。降雨后Cl-值可達到2000~500mg/L。
采用標準曲線計算校正法可不加硫酸汞,準確測定高氯化物廢水CODcr值。此方法與標準方法測定結果相對偏差在7%之內。
2 標準曲線計算校正法
2.1 標準曲線的繪制
(1)原理:
用標準方法測定不同濃度純NaCl水溶液的COD值,將測定的結果繪成標準曲線。
(2)測定步驟:
配制不同濃度的NaCl水溶液,用CODcr標準方法(不加HgSO4)測定水溶液的CODcr(見表1)。
CODcr
序號 Cl 1250 1500 1750 2000 2250 1 281 338 380 445 500 2 289 346 401 450 516 3 284 341 398 453 516 均值 285 342 393 449 510
用y表示CODcr值,x表示Cl- 濃度值,繪制成標準曲線(見圖1)。
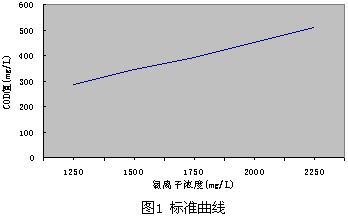
曲線方程: y=0.2228x+5.9
相關系數: r=0.9996
實驗證明氯離子的含量與測得的CODcr值存在良好的線性關系。其斜率為0.2228。
理論計算:2Cl- + 1/2O2 → Cl2↑ + [O]
1mgCl-相當于消耗0.225mg的氧(16/2×35.5=0.225)這與實際結果基本一致。
2.2 測定方法:
(1)原理:將含氯化物的水樣,用重鉻酸鉀標準方法(不加HgSO4)測定的CODcr值寫作CODcr(I)用硝酸銀滴定法,測出水樣中氯離子含量,按標準曲線計算出氯離子含量的CODcr值寫作CODcr(II)該水樣的CODcr值為:
CODcr= CODcr(I)— CODcr(Ⅱ)+α
(2)主要儀器和試劑:
a.儀器:全玻回流裝置(標準磨口500ml三角燒瓶;300mm長的球形冷凝管;電爐;50ml酸式滴定管;10ml、20ml大肚吸管;50ml、100ml量筒。
b.試劑:C(1/6K2Cr2O7)=0.2500mol/LK2Cr2O7標準溶液;C[(NH4)2Fe(SO4)2·6H2O]= 0.1mol/L溶液;試亞鐵靈指示液;濃H2SO4;C(AgNO3)= 0.0141mol/L硝酸銀標準溶液;鉻酸鉀指示液。
(3)測定步驟:
a.CODcr的測定:
吸取20ml水樣于500ml三角燒瓶中,加入0.2500mol/L的重鉻酸鉀溶液10ml,慢慢加入濃H2SO430ml。加熱回流,半小時后停止加熱。略冷后,加入0.3gAgSO4繼續回流1.5小時。冷卻后,用90ml蒸餾水沖洗冷凝管取下三角瓶,溶液總體積不得少于140ml。溶液再度冷卻后,加入三滴試亞鐵靈指示劑,用已標定好的硫酸亞鐵銨標準溶液滴定,溶液的顏色由黃色經藍綠色變為紅褐色即為終點。以20毫升蒸餾水代替水樣,按上述分析步驟求得空白滴定值。
計算公式為:CODCr(mg/L)=[(V0-V1)×C×8×1000]/V2
式中:C—硫酸亞鐵銨標準溶液的濃度(mol/L)
V0—空白消耗硫酸亞鐵銨標準溶液毫升數
V1—水樣消耗硫酸亞鐵銨標準溶液毫升數
V2—取水樣毫升數
注:因為氯化物與硫酸銀生成氯化銀沉淀降低氯化物的化學需氧量,使CODcr(I)值偏低。所以在開始回流的半小時內,重鉻酸鉀將氯化物完全氧化成氯氣后,再加入硫酸銀。
b.氯化物的測定:
取適量水樣,用蒸餾水稀釋至50毫升,置于150毫升三角瓶中,加1毫升鉻酸鉀指示液,用硝酸銀標準溶液滴定至磚紅色沉淀剛剛出現為終點,同時做空白試驗。
氯化物(mg/L)=[(V2-V1)×C×35.45×1000]/V
V1=蒸餾水消耗硝酸銀標準溶液毫升數
V2=水樣消耗硝酸銀標準溶液毫升數
V=水樣毫升數
C=硝酸銀標準溶液濃度(mol/L)
2.3氯化物的干擾:
(1)加硫酸汞消除氯離子干擾法
標準方法中加0.4g硫酸汞絡和水樣的氯離子(氯離子濃度小于2000mg/L)。
HgSO4 + 4Cl- → [HgCl4]2-+ SO42-
K穩= 1.2×1015(25℃)
盡管[HgCl4]-2的穩定常數很大,但仍有少量氯離子存在,能被酸性重鉻酸鉀所氧化,致使測定結果偏高,產生正誤差。
我們對不同濃度氯化物對CODCr的影響進行了試驗。用基準鄰苯二甲酸氫鉀配制已知濃度COD值的水樣,用分析純氯化鈉配制需要的氯化物濃度溶液。根據需要將兩種溶液按不同比例制成混合配水,用標準方法測定(各加0.4g硫酸汞),CODCr測定值>CODCr配制值,其差值即為氯化物與汞絡合后殘存的CODcr值。結果見表2,將其繪制成曲線見圖2。
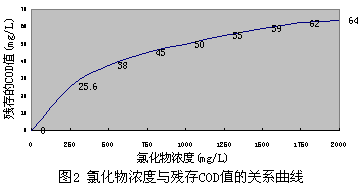
實驗結果表示按標準方法加HgSO4掩蔽氯離子后所測得的CODcr值與不加HgSO4測得CODcr值和0.2228[Cl-]的差值不相等。
CODcr≠COD(I)-0.2228[Cl-]
CODcr=COD(I)-0.2228[Cl-]+α
α為校正系數,就是一小部分未絡合的氯離子產生的COD值,對于配制CODcr=125mg/L(750mg/L<[Cl-]<2000mg/L)的合成水樣α=35+0.0154[Cl-]。
(2)校正系數的計算:
用上述方法對我廠進水、出水,CODcr分別在300-450mg/L和90-130mg/L,[Cl-]在1700-3500mg/L進行了實驗和計算,將合成水樣的α值,用于實際水樣的計算,計算值和實驗值相差很大,說明水樣的氯化物濃度、有機物種類和濃度都影響校正系數α。針對我廠的進水和出水總結出以下兩個公式。
即對于CODcr值在150mg/L以下水樣
α=[Cl-]×1.6/(CODcr(I)-CODcr(II))
通過對21例樣本的計算,CODcr測定的相對偏差6.5%。測定結果見表3。
對于CODcr值在300-450mg/L的水樣
α=[CODcr(I)—CODcr(II)]×0.3
通過對10例樣本計算,CODcr測定的相對偏差5.4%。測定結果見表4:
從我廠試運轉開始至今,共做了三十幾次實驗,數據量不夠大,但找出了影響校正系數α的因素。今后將積累更多數據,完善α值的計算方法,使之有更好的代表性。
3 結論:
1.用重鉻酸鉀法測定CODcr,當水樣中Cl-的濃度較高,COD濃度較低時,用標準法測定COD產生較大誤差,采用標準曲線計算校正法,不加硫酸汞掩蔽氯離子,避免了劇毒藥品HgSO4對環境的污染,可準確測定污水COD值,測定相對誤差小于7%。
2.標準曲線計算校正法中校正系數,與氯化物的濃度,污水中有機物種類和濃度有關,針對不同的水體推導出不同的α值。
參考文獻
1.《水和廢水監測分析方法》 中國環境科學出版社 1998年版
2.《水和廢水監測分析方法指南》 魏復盛 中國環境科學出版社 1994年出版
論文搜索
月熱點論文
論文投稿
很多時候您的文章總是無緣變成鉛字。研究做到關鍵時,試驗有了起色時,是不是想和同行探討一下,工作中有了心得,您是不是很想與人分享,那么不要只是默默工作了,寫下來吧!投稿時,請以附件形式發至 paper@h2o-china.com ,請注明論文投稿。一旦采用,我們會為您增加100枚金幣。








