使用二氧化氯控制THMs
Control of THMs with Chlorine Dioxide
John Newlove Jennifer Miller, Ph.D.Greg D. Simpson, Ph.D.
(Vulcan Performance Chemicals)
張東署 譯
Abstract Chlorine dioxide (ClO2) is effective as both a disinfectant and an oxidant in potable water and wastewater treatment. Its selective reactivity makes chlorine dioxide a powerful oxidizing agent useful in many water treating applications for which chlorine and other oxidizing agents are unsuitable. Unlike chlorine, chlorine dioxide does not react with naturally occurring organic materials to form trihalomethanes (THMs). Chlorine dioxide aids in reducing the formation of Total Trihalomethanes (TTHMs) and haloacetic acids (HAA) by oxidizing THM precursors.
The US EPA’s National Primary Drinking Water Regulations1 set a maximum contaminant level (MCL) of 0.08 mg/L for TTHM.The EPA has identified chlorine dioxide as an alternative or supplemental oxidant-disinfectant that is one of the most suitable for TTHM treatment and control2.
This paper provides a brief overview of THM formation and the use of chlorine dioxide for preventing or controlling THMs. Two case histories are presented.
Keyword Chlorine Dioxide THMs Control
摘要 飲用水和廢水處理中,二氧化氯是一種有效的消毒劑和氧化劑。其選擇性反應特性可以使其作為一種強氧化劑,在氯和其它氧化劑不適用的情況發揮作用。而且與氯不同的是,二氧化氯不會與水中天然存在的一些有機物質發生反應生成三鹵甲烷(THMs)。并且二氧化氯可以通過氧化THMs的母體有機物。從而減少TTHMs(水中總三鹵甲烷量)及HAA(鹵代乙酸)的產生。美國環保總署對于飲用水中TTHMs最大濃度標準為0.08mg/l[1],并且認定在需要對TTHMs進行控制和處理的情況下,二氧化氯可以作為一種替代或補充氧化消毒劑而使用[2]。本文簡要概述了THMs的生產原理及使用二氧化氯控制或減少THMs,并對以往的文獻進行了總結。
關鍵詞 二氧化氯 三鹵甲烷
1. 簡介
估計美國有1200萬人使用的飲用水是由亞氯酸鈉制備出來的二氧化氯消毒的。二氧化氯不但能高度有效地控制飲用水中的水生病原體,而且很少生成鹵化消毒副產物。二氧化氯是一種廣譜殺菌劑,和氯氣一樣,能有效地滅殺病毒、細菌和真菌,二氧化氯對孢子寄生蟲如Giardia和Cryptosporidium滅殺效果要比氯氣好。另外,二氧化氯也能夠有效地去除嗅、味、色、鐵和錳。
1.1 二氧化氯的消毒作用
美國國家基本飲用水管理條例規定[3],飲用水的消毒處理必須確保至少99.9%(3-log)的Giardia lamblia孢子被去除并且/或者滅活;而腸道病毒的去除率并且/或者滅活率至少要達到99.99%(4-log)。只要具備必要的CT值,二氧化氯滅活99.9%的Giardia lamblia孢子和99.99%的腸道病毒是有保證的。此外,美國環保總署最近發布的Stage 2關于微生物和消毒副產物聯邦顧問委員會協議[4]中指出使用二氧化氯來控制Cryptosporidium是一種可以接受的方案。
二氧化氯和氯氣一樣能夠有效地阻止廢水中大腸桿菌的繁殖,而且它對二級出水中病毒的滅殺效果比氯氣好[5]。
1.2 二氧化氯對三鹵甲烷的(THM)控制
二氧化氯與三鹵甲烷的前體腐殖質反應不會生成THMs。在預處理階段用二氧化氯氧化THM的前體,然后氯氣作為消毒劑在凝結、沉淀和過濾后加入。這樣處理后的飲用水比常規氯氣處理所產生的THMs少50-70%。
1.3 二氧化氯對味和嗅的去除
二氧化氯的濃度達到1mg/L時,就能夠有效去除藻類和植物腐爛所產生的味和嗅,二氧化氯能夠氧化低閾值的有異味的化合物,這些化合物包括:二甲萘烷醇,2,3,6-三氯茴香醚(TCA), 2-甲基異冰片(MIB)以及吡嗪類化合物。二氧化氯還能有效去除產生異味的酚類化合物,在此處理過程中,很少產生氯酚[6]。已有試驗證明對于硫醇和有機二硫化合物這類有異味的物質,同樣可以用二氧化氯來氧化去除[7]。
1.4 二氧化氯對鐵和錳的去除
在美國,大約有40%的生活用水中鐵和錳的含量超過推薦的中級最大允許濃度。根據推薦的濃度指標,鐵含量不超過0.3mg/L ,錳含量不超過0.05 mg/L 。之所以這樣規定是因為鐵和錳等于或超過此含量會使水有顏色、渾濁、著色以及口感不佳。鐵和錳也可能會加速分散系統中微生物的生長,進一步惡化水的味、嗅以及色的情況。二氧化氯能快速與溶解于水中鐵和錳反應生成不溶于水的沉淀物,然后可以用沉淀和過濾的方法將沉淀物從水中分離出去。用二氧化氯預氧化鐵和錳同樣能提高其的沉積效果,產生更好的濾出時間[8]。
2. 三鹵甲烷的形式
70年代后期,研究人員指出飲用氯氣處理后的水可能會提高患癌癥的幾率[9][10],潛在的致癌物質就是三鹵甲烷(THMs[11][12])。美國環保總署規定,飲用水中THM的含量不得超過0.1 mg/L 。通過對減少飲用水中三鹵甲烷方法的探討[1][13-15],環保總署在1983提出二氧化氯可以作為控制THMs有效的手段。
更多研究表明:地面水特別是當水中腐殖酸和灰黃霉酸的含量很高時用氯氣處理后,三鹵甲烷的含量會顯著提高。過去由于檢測手段的限制,無法對水中不同成分逐一檢測,因此把它們作為三鹵甲烷總量來測定。隨著檢測手段的提高,現在已經可以對不同的三鹵甲烷進行檢測。用氯氣對飲用水進行處理后,會在水中生成致癌物質,如氯仿、溴二氯甲烷以及其它消毒副產物(DBPs)。
注1: MCLG 表示最大允許濃度期望值
最終的消毒劑及消毒副產物條例(DBPR)規定,飲用水中三鹵甲烷總量的最大允許濃度(MCL)為0.08 mg/L ,并且將此規定延伸至所有相似的水體。此外,最近規定鹵代乙酸的最大允許濃度為0.06 mg/L,目前對各組分的限定范圍見表1。
3.二氧化氯對三鹵甲烷的處理
與氯氣相反,二氧化氯和腐殖質(三鹵甲烷的前體)反應不會生成THMs,盡管在二氧化氯處理后的水中可以檢測到微量的三鹵甲烷,這是由于二氧化氯中所含的痕量氯氣雜質所致。
1976年,Miltner 證明用二氧化氯對飲用水進行消毒只產生極微量的三鹵甲烷[16]。后來在Evansville, Indiana[17]; Hamilton, Ohio[18];Galveston, Texas[19]; Louisville, Kentucky[20]; Davenport Iowa[21]; 和Contra Costa, California[14]等地的現場試驗得到了和Miltner相同的結論。
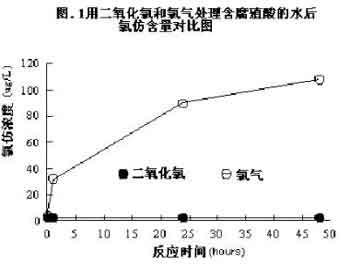
此外,Noack 和Doerr 在1978年作了關于氯氣、二氧化氯以及氯氣和二氧化氯結合起來氧化飲用水中腐殖酸的報道[22]。報道中指出,在二氧化氯濃度不高的情況下,它與水中腐殖酸的反應速率要遠遠小于它在濃度較高時的反應速率,正如所預料的是與氯氣不同,二氧化氯與腐殖酸反應不會產生氯仿。試驗結果如圖1所示。
1984年,Rav-Acha 發現許多前期關于二氧化氯產生氯化有機物(包括三鹵甲烷)的研究工作過高地估計了二氧化氯在正常投加濃度下所產生氯化有機物的量[15]。他報道在通常的二氧化氯使用條件下處理后的飲用水中檢測不到THMs,這與Miltner[16], Henderson等人[23], 和Miller等人[13]的試驗結果吻合。他指出二氧化氯消毒所產生的主要是氧化副產物而不是氯化副產物。他同樣注意到二氧化氯與氯氣相比,在天然水中選擇性更高而且相對氯氣而言,二氧化氯投加濃度一定。
Lykins在1986年報道,用二氧化氯預處理可以減少飲用水中三鹵甲烷的含量[24]。在二氧化氯預處理以前,三鹵甲烷的總含量是141 μg/L ,處理后總含量降至1.4 μg/L 。二氧化氯處理后的水用GC-MS分析,未檢測到氯化副產物。在其它水處理廠也得到了同樣的結果[25]。
ndrews[26]最近在加拿大使用二氧化氯進行消毒實驗, 結果表明用氯氣消毒后TTHMs為30 μg/L,而二氧化氯處理后TTHMs為5μg/L以下,用二氧化氯處理后,鹵代乙酸(HAA’s)由氯氣消毒后的20μg/L以上降為8μg/L以下;此外,對Giardia的滅殺率也從90%以下提高到99.9%。這說明在水中殘余的二氧化氯仍然具有很好的消毒效果。
總而言之,二氧化氯消毒機理為氧化反應[27][28]。氯氣除了氧化反應以外,還有很大一部分發生了副反應[23],其結果就是產生了鹵代有機物,如三鹵甲烷。人們研究了很多方法來去除由于氯氣消毒所產生的三鹵甲烷,二氧化氯是一種行之有效的方法,能夠從本質上減少三鹵甲烷的形成。
3.1 二氧化氯投加量
二氧化氯一般在原水中的投加濃度范圍為0.1到5.0 mg/L。對大多數城市用水以及其它飲用水系統而言,為了保證消毒效果,需要二氧化氯在水中的余量達到2.0mg/L。處理后的水中也可以投加二氧化氯來保持消毒劑一定的殘留量。二氧化氯投加的量與水本身的狀況、污染程度以及處理級別有關系。美國飲用水基本管理條例和州飲用水標準規定,必須對水中殘余的消毒劑和消毒副產物進行監測。對于工業廢水和生活污水的處理而言,要保證其處理效果,一般認為二氧化氯的殘余量應達到5mg/L。
3.2 二氧化氯投加方法
二氧化氯是由亞氯酸鈉和一種氧化劑或者一種酸性介質反應制備出來的氣體物質。通過二氧化氯發生器將亞氯酸鈉轉化為二氧化氯,然后稀釋成二氧化氯溶液后使用。應該在處理系統中選擇一個適當的地點投加二氧化氯,這是為了使加入的二氧化氯可以得到充分的混合并且在系統中均勻的分布。投加藥劑的地點應該位于水位線以下,這可以防止二氧化氯揮發。不要把亞氯酸鈉直接投加到飲用水中。
3.3 二氧化氯的分析
消毒副產物管理條例(DBPR)規定:除了對消毒副產物監測以外,對二氧化氯作消毒劑或氧化劑的飲用水系統中所含的二氧化氯以及亞氯酸根也要進行監測。盡管這些規定和方法未必適用于其它國家,但在美國這些規定是完整的。
二氧化氯:在美國,監測二氧化氯的余量建議采用下列兩種方法(詳見《水和廢水標準測試方法》第20版)之一:
DPD 法,4500-ClO2 D
電流滴定法II,4500-ClO2 E[29]
上述方法是政府部門推薦的監測方法,還可以采用DPD比色法測試裝置來測量系統中消毒劑二氧化氯的余量。
亞氯酸鈉:對于水中亞氯酸根的監測而言,必須采用下面所推薦的三種方法(詳見《水和廢水標準測試方法》第20版)之一:
電流滴定法II,4500-ClO2 E
離子色譜法,EPA法300.0[30]
離子色譜法,EPA 法300.1[31]
特別規定電流滴定法可以用于對加藥點亞氯酸根濃度的日常監測,但是對于系統內部亞氯酸根每月的或者附加的監測必須采用離子色譜法。
4.應用實例
4.1 實例1:二氧化氯對嗅和味的去除及其對三鹵甲烷的控制
美國某大城市,每天消毒處理的飲用水量為1200萬-3600萬加侖。水中富含100多種有嗅和味的物質,水廠為此感到很頭痛。過去對進入水廠原水進行處理的消毒劑主要是氯氣,結果消毒后的水中THMs 含量相當高,因此需要找到一種消毒劑來取代氯氣,要求該消毒劑不但能夠有效地去除水的嗅和味、抑制THM的產生,而且具有足夠的消毒效果。
有人建議市政當局用二氧化氯來處理原水,采用Rio LindaÒ公司生產的雙組分流動發生器(加料速度為1.75-2.0 mg/L)對原水進行處理,結果證明二氧化氯的效果確實很好。
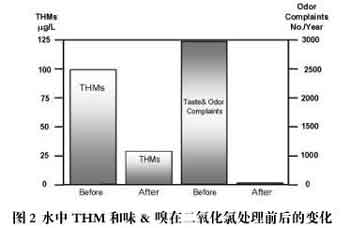
原水經過二氧化氯處理后,嗅和味明顯地減少了,同時飲用水中THMs的含量甚至下降到美國環保總署規定的指標以下。另外,二氧化氯在水廠中使用結果顯示它的消毒性能也很好。二氧化氯從1998年開始作為飲用水消毒劑,而且公眾對它消毒效果非常滿意。圖2表示飲用水用二氧化氯處理前后的嗅和味及三鹵甲烷的變化。
4.2 實例2:使用二氧化氯控制城市飲用水中的THMs
在美國東南部某市,每天有3300萬加侖的飲用水經過消毒處理,過去對進入水廠原水進行處理的消毒劑主要是氯氣,結果消毒后的飲用水中THMs 含量相當高,因此需要找到一種消毒劑來取代氯氣,要求該消毒劑不但具有足夠的消毒效果,而且能夠有效地抑制THM的產生。
有人建議市政當局用二氧化氯來處理原水,采用Rio LindaÒ公司生產的雙組分流動發生器(加料速度為0.5mg/L)對原水進行處理,還有人建議氯氣可作為消毒劑在后續階段使用。
二氧化氯能夠有效降低飲用水中THMs的含量,甚至可以使其降低到美國環保總署規定的指標以下。運用二氧化氯處理的其他好處是:控制鐵和錳的含量;在消毒的同時能氧化有異味的物質。二氧化氯從1992年開始作為飲用水消毒劑,而且公眾對它消毒效果非常滿意。圖3表示飲用水用二氧化氯處理前后三鹵甲烷含量的變化。

4.3 結論
在飲用水處理中,二氧化氯已被確證為一種有效的抑制或減少THMs生成的方法。此外,二氧化氯用在飲用水的前處理和后處理階段,能夠有效控制水的味和嗅以及去除水中的鐵和錳。
作為氯氣的替代品,二氧化氯不僅經濟而且有效。因此,美國環保總署已把二氧化氯列為可替代或補充的用于處理和控制TTHM的最佳氧化—消毒劑之一[2]。
參考文獻
1. Federal Register, National Primary Drinking Water Regulations: Disinfectants and Disinfection Byproducts, 63 FR 69389 (December 16, 1998).
2. USEPA, “Alternative Disinfectants and Oxidants Guidance Manual “EPA/815/R-99/014, (April 1999).
3. Code of Federal Regulations, National Primary Drinking Water Regulations, Subpart H – Filtration and Disinfection. 40 CFR 141.70-.75.
4. Federal Register, Stage 2 Microbial and Disinfection Byproducts Federal Advisory Committee Agreement in Principal(Stage 2 M-DBP Agreement), 65FR83015, (December 29, 2000).
5. Roberts, P.V., Aieta, E.M., Berg, J.D., and Chow. B.M., “Chlorine Dioxide for Wastewater Disinfection: A Feasibility Evaluation,” Stanford University, EPA-600/2-81-092 (1981).
6. Lalezary, S., Pirbdzdri, M., Mc.Guire, M.J., “Oxidation of Five Earthy-Musty Taste and Odor Compounds”, JAWWA, 62-69, (March 1986).
7. Warf, C.C. Jr., “Chlorine Dioxide and The Small Drinking Water System”, published in Providing Safe Drinking Water in Small Drinking Water Systems, Lewis Publishers, 121-131 (1998).
8. Stevens, A.A., “Reaction of Chlorine Dioxide”, Environ. Health Perspect., 46;101 (1982)
9. Alavanja, M., Goldstein I., and Sasser, M., "A Case Control Study of Gastrointestinal and Urinary Tract Cancer Mortality and Drinking Water Chlorination, in Water Chlorination,” in Environmental Impact and Health Effects, (edited by Jolley, R. L.), Vol. 2, pp. 395. Ann Arbor Science, Ann Arbor, MI., 1980.
10. Page, T., Harris, R. H., and Epstein, S. S., "Drinking Water and Cancer Mortality in Louisiana," Science 193, 55 (1976).
11. Report of the Carcinogenesis Bioassay of Chloroform. NTIS PB264018/AS, National Cancer Institute, 1976.
12. Roe, F. J. C., "Preliminary Report of Long-Term Tests of Chloroform in Rats, Mice and Dogs," unpublished Report. Cited in Ozone, Chlorine Dioxide and Chloramines as alternatives to Chlorine for Disinfection of Drinking Water. Water Supply Research, Office of Research and Development, U.S. EPA, Cincinnati, OH, 1976.
13. Miller, G. W., Rice, R. G., Robson, C. M., Kuhn, W., and Wolf, H., "An Assessment of Ozone and Chlorine Dioxide Technologies for Treatment of Municipal Water Supplies," EPA Report 600012-78-147, Cincinnati, OH, 1978.
14. Lange, A., and E. Kawczynski, 1978, "Controlling Organics, the Contra Costa County Water District," JAWWA 70:653.
15. Rav-Acha, Ch., 1984, “The Reactions of Chlorine Dioxide with Aquatic Organic Materials and Their Health Effects,” Water Res., 18(11):84.
16. Miltner, R. J., 1976, "The Effect of Chlorine Dioxide on Trihalomethanes in Drinking Water," MS Thesis, University of Cincinnati.
17. Lykins, B.W., Jr. and Griese, M.H., "Using Chlorine Dioxide for Trihalomethane Control," JAWWA, 78, 88 (1986).
18. Augenstein, H.W., "Use of Chlorine Dioxide to Disinfect Water Supplies," JAWWA, 66, 716 (1974).
19. Myers, G.L., et al., "Control of Trihalomethanes and Taste and Odor at Galveston County Water Authority," Proc. Annual Meeting, AWWA, at Denver, CO, 1667-1675 (1986).
20. Hubbs, S. A., M. Guers, and J. Siria, 1980, "Plant-scale Examination and Control of a ClO2-Chloramination Process at the Louisville Water Company," in Water Chlorination: Environmental Impact and Health Effects, Vol 3., Jolley, R. L., et. al., eds, Ann Arbor Science Publishers, Ann Arbor, Michigan.
21. Blanck, C., 1979, "Trihalomethane Reduction in Operating Water Treatment Plants," JAWWA 71:525.
22. Noack, M. G., and R. L. Doerr, 1978, “Reactions of Chlorine, Chlorine Dioxide and Mixtures Thereof with Humic Acid: An Interim Report.,” in Water Chlorination: Environmental Impact and Health Effects, Vol. 2., (R. L. Jolley, et. al., editors), Ann Arbor Science. Ann Arbor, MI.
23. Henderson, J. E., G. R. Peyton, and W. H. Glaze, 1976, “A Convenient Liquid-Liquid Extraction Method for the Determination of Halomethanes in Water at the ppb Level,” in Identification and Analysis of Organic Pollutants in Water, edited by Keith, L. H., Ann Arbor Science, Ann Arbor, MI., 105.
24. Lykins, B. W., and M. H. Griese, June 1986, “Using Chlorine Dioxide for Trihalomethane Control,” JAWWA 78:6:88.
25. Lykins, B. W., and W. Koffskey, August 1985, “Products Identified at an Alternative Disinfection Pilot Plant,” 2nd International Symposium on Health Effects of Drinking Water Disinfectants and Disinfection Byproducts, Cincinnati, OH.
26. Andrews, R. et al.,“Chlorine Dioxide Trial as a Post Disinfectant in Wiarton, Ontario, Fourth Int.Symp.International Symposium on Chlorine Dioxide, February 15-16, Las Vegas, Nevada (2001).
27. Synan, J.F., 1979, “Chlorine Dioxide - An Effective Biocide for Recycled or Reused Water Systems,” Trans. Citrus Eng. Conf., 25:66.
28. Rav-Acha, Ch., and R. Blits, 1985, “The Different Reaction Mechanisms by Which Chlorine and Chlorine Dioxide React with Polycyclic Aromatic Hydrocarbons (PAH) in Water,” Water Research, 19(10):1273.
29. Standard Methods for the Examination of Water and Wastewater, APHA, AWWA and WEF, Washington, D.C. (20th Ed. l998).
30. Methods for the Determination of Inorganic Substances in Environmental Samples. USEPA. 1993. EPA/600/R-93/100.
31. USEPAMethod 300.1, Determination of Inorganic Anions in Drinking Water by Ion Chromatography, Revision 1.0. USEPA. 1997. EPA/600/R-98/118
論文搜索
月熱點論文
論文投稿
很多時候您的文章總是無緣變成鉛字。研究做到關鍵時,試驗有了起色時,是不是想和同行探討一下,工作中有了心得,您是不是很想與人分享,那么不要只是默默工作了,寫下來吧!投稿時,請以附件形式發至 paper@h2o-china.com ,請注明論文投稿。一旦采用,我們會為您增加100枚金幣。








